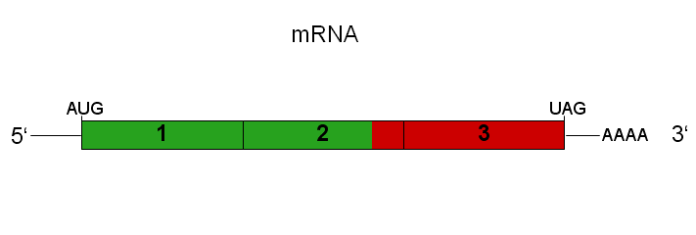
בניגוד ל-mRNA רגיל חיסונים שמקודד רק לאנטיגנים של המטרה, ה-mRNA המגבירים את עצמם (saRNAs) מקודדים לחלבונים לא מבניים ומקדם גם מה שגורם saRNAs רפליקונים המסוגלים לשעתוק in vivo בתאי המארח. תוצאות מוקדמות מצביעות על כך שהיעילות שלהם, כאשר ניתנת במינונים קטנים יותר, שווה לזו של מינונים רגילים של קונבנציונליות. mRNA. עקב דרישות מינון נמוך, פחות תופעות לוואי ומשך פעולה ארוך יותר, saRNA מופיעה כפלטפורמת RNA טובה יותר עבור חיסונים (כולל עבור v.2.0 של חיסוני mRNA COVID) ותרופות חדשות יותר. עדיין לא אושר חיסון או תרופה מבוססי saRNA לשימוש אנושי. עם זאת, להתקדמות משמעותית בתחום זה יש פוטנציאל להוביל מחדש את המניעה והטיפול בזיהומים והפרעות ניווניות.
מיותר לציין שהאנושות שברירית לפני מגיפות כמו COVID. כולנו חווינו את זה והושפענו מזה בצורה כזו או אחרת; מיליונים לא יכלו לחיות כדי לראות את הבוקר שלמחרת. בהינתן שגם לסין הייתה תוכנית חיסונים ענקית ל-COVID-19, הדיווחים האחרונים בתקשורת על קפיצות של מקרים ותמותה בבייג'ינג וסביבתה מדאיגים. הצורך בהיערכות ובמרדף בלתי פוסק אחר יעיל יותר חיסונים ואי אפשר להמעיט בטיפולים.
המצב יוצא הדופן שהציג מגיפת COVID-19 סיפק הזדמנות למבטיחים רנ"א טכנולוגיה לצאת מהגיל. ניתן היה להשלים ניסויים קליניים בקצב שיא ו mRNA מבוסס COVID חיסונים, BNT162b2 (מיוצר על ידי Pfizer/BioNTech) ו mRNA-1273 (על ידי Moderna) קיבלה EUA מהרגולטורים, ובבוא העת, מילא תפקיד חשוב במתן הגנה מפני המגיפה לאנשים במיוחד באירופה ובצפון אמריקה1. ה-mRNA האלה חיסונים מבוססים על פלטפורמות RNA סינתטיות. זה מאפשר ייצור תעשייתי מהיר, ניתן להרחבה וללא תאים. אבל אלה אינם נטולי מגבלות כגון עלות גבוהה, שרשרת אספקה קרה, ירידת טיטר נוגדנים, אם להזכיר כמה.
mRNA חיסונים כרגע בשימוש (המכונה לפעמים קונבנציונלי או דור 1 mRNA חיסונים) מבוססים על קידוד האנטיגן הנגיפי ב-RNA סינתטי. מערכת מסירה לא ויראלית מעבירה את התמליל לציטופלזמה של התא המארח, שם מתבטא האנטיגן הנגיפי. האנטיגן המובע לאחר מכן גורם לתגובה חיסונית ומספק חסינות פעילה. מכיוון ש-RNA מתפרק בקלות ו-mRNA זה בחיסון אינו יכול לתמלל את עצמו, יש צורך לתת כמות ניכרת של תמלול RNA ויראלי סינתטי (mRNA) בחיסון כדי לעורר תגובה חיסונית רצויה. אבל מה אם תעתיק ה-RNA הסינטטי משולב גם עם חלבונים לא מבניים וגנים מקדמים, בנוסף לאנטיגן הנגיפי הרצוי? כמו רנ"א לתמלול תהיה יכולת לתמלל או להגביר את עצמו כאשר הוא מועבר לתא המארח למרות שהוא יהיה ארוך יותר וכבד יותר וההעברה שלו לתאי המארח עשויה להיות מורכבת יותר.
שלא כמו קונבנציונלי (או, לא מגביר) mRNA שיש לו קודים רק לאנטיגן הנגיפי הממוקד, ההגברה העצמית mRNA (saRNA), יש יכולת לתמלל את עצמו כאשר הוא נמצא בתאי המארח ב-vivo בזכות נוכחותם של קודים נדרשים לחלבונים לא מבניים ולפרומוטור. מועמדים לחיסון mRNA המבוססים על mRNA מגבירים עצמיים נקראים הדור השני או הבא mRNA חיסונים. אלה מציעים הזדמנויות טובות יותר במונחים של דרישות מינון נמוכות יותר, יחסית פחות תופעות לוואי ומשך פעולה/השפעות ארוך יותר (2-5). שתי הגרסאות של פלטפורמת RNA ידועות לקהילה המדעית מזה זמן מה. בתגובה למגיפה, החוקרים בחרו בגרסה שאינה משכפלת של פלטפורמת mRNA לפיתוח חיסונים לאור הפשטות והדרישות של מצב המגיפה וכדי לצבור ניסיון עם גרסה שאינה מגבירה תחילה כפי שהיתר זהירות. עכשיו, יש לנו שני mRNA מאושרים חיסונים נגד COVID-19, ומספר מועמדים לחיסון וטיפול בצנרת כגון חיסון נגד HIV וטיפול ב מחלת שארקו-מארי-שן.
מועמדים לחיסון saRNA נגד COVID-19
העניין בחיסון saRNA אינו חדש במיוחד. בתוך כמה חודשים מתחילת המגיפה, באמצע 2020, מקיי ואח'. הציג מועמד חיסון מבוסס saRNA שהראה כימי נוגדנים גבוהים בסרת עכברים וניטרול טוב של הנגיף6. הניסוי הקליני שלב 1 של VLPCOV-01 (הגברה עצמית רנ"א מועמד לחיסון) על 92 מבוגרים בריאים שתוצאותיהם פורסמו בהדפסה מוקדמת בחודש שעבר הגיעו למסקנה כי מתן מינון נמוך של זה saRNA מועמד חיסון מושרה תגובה חיסונית דומה לחיסון ה-mRNA המקובל BNT162b2 וממליץ על המשך פיתוחו כחיסון מאיץ7. במחקר אחר שפורסם לאחרונה, שנערך כחלק מהניסוי הקליני COVAC1 לפיתוח אסטרטגיית מתן מינון דחף, נמצאה תגובה חיסונית מעולה אצל אנשים שסבלו בעבר עם COVID-19 וקיבלו הגברה עצמית חדשה. רנ"א (saRNA) חיסון נגד COVID-19 בתוספת חיסון מורשה בבריטניה8. ניסוי פרה-קליני של מועמד חיסון פומי חדש המבוסס על הגברה עצמית רנ"א במודל עכבר העלה טיטר נוגדנים גבוה9.
מועמד לחיסון saRNA נגד שפעת
שפעת חיסונים כיום בשימוש מבוססים על וירוסים מומתים או רקומביננטי סינתטי (גן HA סינתטי בשילוב עם בקולובירוס)10. הגברה עצמית mRNAמועמד חיסון מבוסס עשוי לעורר חסינות נגד אנטיגנים ויראליים מרובים. ניסוי פרה-קליני של מועמד לחיסון sa-mRNA bicistronic A/H5N1 נגד שפעת על עכברים וחמוסים העלה תגובה חזקה של נוגדנים ותאי T, המצדיקה הערכה על בני אדם בניסויים קליניים11.
חיסונים נגד COVID-19 זכו לתשומת לב ממוקדת מסיבות ברורות. כמה עבודות פרה-קליניות ליישום פלטפורמות RNA נעשו עבור זיהומים אחרים והפרעות לא מדבקות כגון סרטן, מחלת אלצהיימר והפרעות תורשתיות; עם זאת, עדיין לא אושרו חיסון או תרופה מבוססי saRNA לשימוש אנושי. יש לבצע מחקר נוסף על השימוש בחיסונים מבוססי saRNA על מנת להבין באופן מקיף את בטיחותם ויעילותם לשימוש בבני אדם.
***
הפניות:
- Prasad U., 2020. חיסון mRNA COVID-19: אבן דרך במדע ומשנה משחק ברפואה. אירופאי מדעי. פורסם ב-29 בדצמבר 2020. זמין באינטרנט בכתובת http://scientificeuropean.co.uk/medicine/covid-19-mrna-vaccine-a-milestone-in-science-and-a-game-changer-in-medicine/
- Bloom, K., Van den Berg, F. & Arbuthnot, P. חיסוני RNA להגברה עצמית למחלות זיהומיות. ג'ין תר 28, 117-129 (2021). https://doi.org/10.1038/s41434-020-00204-y
- פורסייף מ.מ ואח' 2022. חיסוני mRNA מגבירים עצמיים: אופן פעולה, עיצוב, פיתוח ואופטימיזציה. גילוי סמים היום. כרך 27, גיליון 11, נובמבר 2022, 103341. DOI: https://doi.org/10.1016/j.drudis.2022.103341
- בליקני AK ואח' 2021. עדכון על פיתוח חיסון mRNA מגביר עצמי. חיסונים 2021, 9(2), 97; https://doi.org/10.3390/vaccines9020097
- אנה בלקני; הדור הבא של חיסוני RNA: RNA מגביר עצמי. Biochem (Lond) 13 באוגוסט 2021; 43 (4): 14–17. דוי: https://doi.org/10.1042/bio_2021_142
- McKay, PF, Hu, K., Blakney, AK et al. מועמד לחיסון ננו-חלקיקי שומנים ל-RNA SARS-CoV-2 מגביר עצמי משרה כימי נוגדנים מנטרלים גבוהים בעכברים. Nat Commun 11, 3523 (2020). https://doi.org/10.1038/s41467-020-17409-9
- Akahata W., et al 2022. בטיחות ואימונוגניות של חיסון RNA מגביר עצמי של SARS-CoV-2 המבטא RBD מעוגן: מחקר שלב 1 אקראי, עיוור צופה. Preprint medRxiv 2022.11.21.22281000; פורסם ב-22 בנובמבר 2022. doi: https://doi.org/10.1101/2022.11.21.22281000
- אליוט T, et al. (2022) תגובות חיסוניות משופרות בעקבות חיסון הטרולוגי עם חיסוני RNA ו-mRNA COVID-19 מגבירים עצמיים. PLoS Pathog 18(10): e1010885. פורסם: 4 באוקטובר 2022. DOI: https://doi.org/10.1371/journal.ppat.1010885
- Keikha, R., Hashemi-Shahri, SM & Jebali, A. ההערכה של חיסונים אוראליים חדשים המבוססים על חלקיקי שומנים RNA בעלי הגברה עצמית (saRNA LNPs), LNPs Lactobacillus plantarum שעברו saRNA, ו-saRNA שעברו transfected Lactobacillus SARS-plantarum כדי לנטרל. -2 גרסאות אלפא ודלתא. Sci Rep 11, 21308 (2021). פורסם: 29 באוקטובר 2021. https://doi.org/10.1038/s41598-021-00830-5
- CDC 2022. כיצד נוצרים חיסונים נגד שפעת. זמין באינטרנט ב https://www.cdc.gov/flu/prevent/how-fluvaccine-made.htm גישה אליו ב -18 בדצמבר 2022.
- Chang C., et al 2022. חיסוני שפעת bicistronic mRNA בעלי הגברה עצמית מעלים תגובות חיסוניות צולבות בעכברים ומונעים זיהום בחמוסים. שיטות טיפול מולקולרי ופיתוח קליני. כרך 27, 8 בדצמבר 2022, עמודים 195-205. https://doi.org/10.1016/j.omtm.2022.09.013
***