בני אדם לא היה קיים בלעדיו וירוסים כי חלבון ויראלי ממלא תפקיד מפתח בפיתוח של בן אנוש עוּבָּר. עם זאת, לפעמים הם מהווים איומים קיומיים בצורה של מחלות כמו במקרה של מגיפת COVID-19 הנוכחית. באופן אירוני, וירוסים מהווים ~8% מהגנום שלנו, שנרכש במהלך האבולוציה, מה שהופך אותנו ל"כמירה כמעט".
המילה הידועה לשמצה והנוראה ביותר של שנת 2020 ללא ספק היא 'וירוס'. הרומן וירוס אחראית למחלת COVID-19 חסרת התקדים הנוכחית וכמעט כמעט קריסה של הכלכלה העולמית. כל זה נגרם על ידי חלקיק זעיר שאפילו אינו נחשב כחי "במלא" מכיוון שהוא נמצא במצב לא תפקודי מחוץ למארח, תוך שהוא מנציח רק בפנים עם הדבקה של המארח. מפתיעה ומזעזעת יותר היא העובדה שה בני אדם נושאים את ה"גנים" הנגיפיים מאז ומעולם וכיום גנים ויראליים מהווים ~8% מה בן אנוש גנום (1). רק כדי לשים את זה בפרספקטיבה, רק ~1% בן אנוש הגנום פעיל פונקציונלית אחראי לייצור חלבונים שקובעים מי אנחנו.
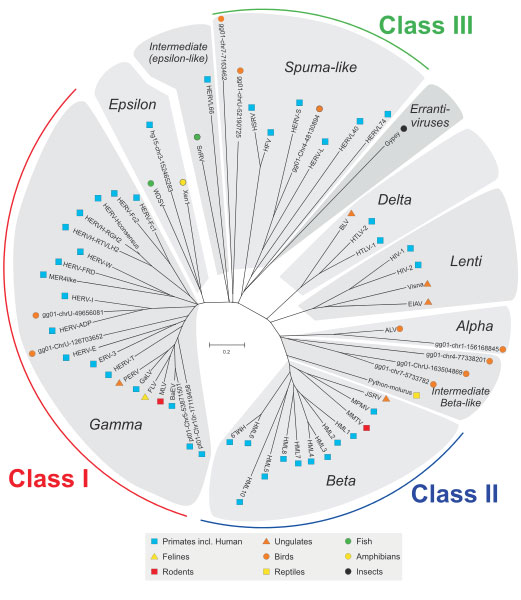
סיפור היחסים בין בני אדם ו וירוסים התחיל לפני 20-100 מיליון שנה כאשר אבותינו נדבקו על ידי וירוסים. כל משפחת רטרו-וירוס אנדוגנית נגזרת מזיהום בודד של תאי קו הנבט על ידי רטרו-וירוס אקסוגני שלאחר השתלבות באבותינו, התרחב והתפתח (2). הריבוי שלאחריו ההעברה האופקית מההורים לצאצאים וכיום יש לנו הגנום הנגיפי הזה מוטבע ב-DNA שלנו. בן אנוש רטרו-וירוס אנדוגניים (HERVs). זהו תהליך מתמשך ואולי אפילו קורה כרגע. במהלך האבולוציה, HERVs אלה רכשו מוטציות, התייצבו ב- בן אנוש הגנום ואיבדו את יכולתם לגרום למחלה. האנדוגני רטרו-וירוסים לא נמצאים רק ב בני אדם אך נמצאים בכל היצורים החיים. כל הרטרו-וירוסים האנדוגניים הללו המקובצים לשלוש מחלקות (Class I, II ו-III) המתרחשים על פני מיני בעלי חיים שונים מציגים קשר פילוגנטי המבוסס על דמיון הרצף שלהם (3) כפי שמתואר באיור למטה. HERVs שייכים לקבוצת Class I.
מבין רטרו-וירוסים המשובצים השונים הקיימים ב- בן אנוש הגנום, דוגמה קלאסית שכדאי להזכיר כאן, היא של חלבון רטרו-ויראלי שהוא חלבון מעטפת פיוגני ביותר בשם סינציטין, (5) שתפקידו המקורי ב- וירוס היה להתמזג עם תאי מארח כדי לגרום לזיהום. החלבון הזה הותאם כעת בני אדם ליצור שליה (איחוי תאים ליצירת תאים מרובי גרעינים) שלא רק מספקת מזון לעובר מהאם במהלך ההריון אלא גם מגנה על העובר מפני המערכת החיסונית של האם בשל האופי המדכא את החיסון של חלבון הסינסיטין. HERV הספציפי הזה הוכח כמועיל ל בן אנוש גזע על ידי הגדרת עצם קיומו.
HERVs היו מעורבים גם במתן חסינות מולדת למארח על ידי מניעת זיהום נוסף וירוסים או הפחתת חומרת המחלה עם הדבקה חוזרת בסוג דומה של וירוסים. סקירה משנת 2016 של קצוראקיס ואסוואד (6) מתארת את זה אנדוגני וירוסים יכול לשמש כאלמנטים רגולטוריים לגנים השולטים בתפקוד החיסון, ובכך להוביל להתפתחות חסינות. באותה שנה, Chuong וחב' (7) הדגימו כי HERVs מסוימים פועלים כמשפרי רגולציה על ידי אפנון הביטוי של גנים הניתנים להשראת IFN (אינטרפרון) ובכך מספקים חסינות מולדת. מוצרי ביטוי HERV יכולים לפעול גם כדפוסים מולקולריים הקשורים לפתוגן (PAMPs), לעורר את הקולטנים התאיים האחראים לקו ההגנה הראשון של המארח (8-10).
היבט מעניין נוסף של HERVs הוא שחלקם מראים פולימורפיזמים של החדרה, כלומר מספר שונה של עותקים קיימים בגנום עקב אירועי החדרה. מחקר של 20 נבדקים המשתייכים לקבוצות אתניות שונות גילה דפוסי פולימורפיזם של החדרה בין 0-87% בכל הנבדקים (11). יכולות להיות לכך השלכות בגרימת מחלות על ידי הפעלה של גנים מסוימים שקטים אחרת.
כמו כן, הוכח כי HERVs מסוימים קשורים להתפתחות של הפרעות אוטואימוניות כגון טרשת נפוצה (12). בתנאים פיזיולוגיים נורמליים, ביטוי HERV מווסת בצורה הדוקה בעוד שבתנאים פתולוגיים הנובעים משינויים בסביבה החיצונית/פנימית, שינויים הורמונליים ו/או אינטראקציה מיקרוביאלית עלולים לגרום לחוסר ויסות של ביטוי HERV, המוביל למחלה.
המאפיינים לעיל של HERVs מצביעים על כך שלא רק נוכחותם ב בן אנוש הגנום הוא בלתי נמנע, אבל יש להם את היכולת לווסת את ההומאוסטזיס של מערכת החיסון על ידי הפעלה או דיכוי שלה, ובכך לגרום להשפעות דיפרנציאליות (מהיותן מועילות לגרימת מחלה) במארחים.
מגיפת COVID-19 נגרמת גם על ידי רטרו-וירוס SARS-nCoV-2, השייך למשפחת השפעת, וייתכן שסביר שבמהלך האבולוציה, גנומים הקשורים למשפחה זו של וירוסים השתלב ב בן אנוש הגנום ונמצאים כעת כ- HERVs. ההנחה היא ש- HERVs אלה עשויים להפגין פולימורפיזמים שונים, כפי שהוזכר לעיל, בקרב אנשים ממוצא אתני שונה. פולימורפיזמים אלה עשויים להיות בצורה של מספר העתקות דיפרנציאלי של HERVs אלה ו/או נוכחות או היעדר מוטציות (שינויים ברצף הגנום) שנצברו לאורך תקופה. שונות זו ב-HERVs המשולבים עשויה להציע הסבר לשיעורי התמותה הדיפרנציאליים ולחומרת מחלת COVID-19 במדינות שונות המושפעות מהמגיפה.
***
הפניות:
1. Griffiths DJ 2001. Endogenous retroviruses in the בן אנוש רצף הגנום. גנום ביול. (2001); 2(6) ביקורות 1017. DOI: https://doi.org/10.1186/gb-2001-2-6-reviews1017
2. Boeke, JD; Stoye, JP (1997). "רטרוטרנספוזונים, רטרו-וירוסים אנדוגניים והאבולוציה של רטרו-אלמנטים". בארון, JM; יוז, SH; Varmus, HE (עורכים). רטרו-וירוסים. Cold Spring Harbor Laboratory Press. PMID 21433351.
3. Vargiu L, et al. סיווג ואפיון של בן אנוש רטרו-וירוסים אנדוגניים; צורות פסיפס נפוצות. רטרוווירולוגיה (2016); 13: 7. DOI: 10.1186 / s12977-015-0232-y
4. Classes_of_ERVs.jpg: Jern P, Sperber GO, Blomberg J (עבודה נגזרת: Fgrammen (שיחה)), 2010. זמין באינטרנט בכתובת https://commons.wikimedia.org/wiki/File:Classes_of_ERVs.svg נגיש ב-07 במאי 2020
5. בלונד, JL; לאווילט, ד; Cheynet, V; בוטון, או; אוריול, ג; Chapel-Fernandes, S; מנדרנדס, ס; מאלט, פ; Cosset, פלורידה (7 באפריל 2000). "גליקופרוטאין מעטפת של ה בן אנוש אנדוגני רטרווירוס HERV-W מתבטא בשליה האנושית וממזג תאים המבטאים את הקולטן של רטרו-וירוס יונקים מסוג D". J. Virol. 74 (7): 3321–9. DOI: https://doi.org/10.1128/jvi.74.7.3321-3329.2000.
6. קצוראקיס א' ואסוואד א' אבולוציה: אנדוגנית וירוסים ספק קיצורי דרך בחסינות אנטי-ויראלית. ביולוגיה נוכחית (2016). 26: R427-R429. http://dx.doi.org/10.1016/j.cub.2016.03.072
7. Chuong EB, Elde NC ו-Feschotte C. אבולוציה רגולטורית של חסינות מולדת באמצעות שיתוף פעולה של רטרו-וירוסים אנדוגניים. מדע (2016) כרך. 351, גיליון 6277, עמ' 1083-1087. DOI: https://doi.org/10.1126/science.aad5497
8. Wolff F, Leisch M, Greil R, Risch A, Pleyer L. החרב הפיפיות של (מחדש) ביטוי של גנים על ידי תרופות היפו-מתילציות: מחיקוי ויראלי ועד לניצול כסוכני התחלות לאפנון ממוקד של נקודת ביקורת חיסונית. Cell Commun Signal (2017) 15:13. DOI: https://doi.org/10.1186/s12964-017-0168-z
9. Hurst TP, Magiorkinis G. הפעלה של התגובה החיסונית המולדת על ידי אנדוגני רטרו-וירוסים. J Gen Virol. (2015) 96:1207–1218. DOI: https://doi.org/10.1099/vir.0.000017
10. Chiappinelli KB, Strissel PL, Desrichard A, Chan TA, Baylin SB, Correspondence S. Inhibiting DNA methylation גורם לתגובת אינטרפרון בסרטן דרך dsRNA כולל רטרו-וירוסים אנדוגניים. תא (2015) 162:974–986. DOI: https://doi.org/10.1016/j.cell.2015.07.011
11. Mehrab G, Sibel Y, Kaniye S, Sevgi M ו-Nermin G. Human endogenous רטרווירוס-הקרנת החדרה. דוחות רפואה מולקולרית (2013). DOI: https://doi.org/10.3892/mmr.2013.1295
12. Gröger V, ו-Cynis H. Human Endogenous Retroviruses ותפקידם המשוער בהתפתחות של הפרעות אוטואימוניות כגון טרשת נפוצה. מיקרוביול קדמי. (2018); 9: 265. DOI: https://doi.org/10.3389/fmicb.2018.00265
***